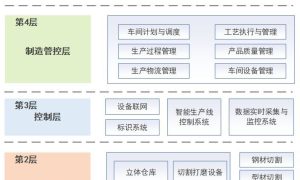
船舶在海洋环境中,难免会发生腐蚀。但是在船舶设计中往往已经考虑到腐蚀余量,而且船腐蚀了也不过是表面有锈迹,影响美观,就算不刷涂料,碳钢每年的腐蚀速率也不过是0.5mm左右,相较于动辄10mm以上厚度的钢板,似乎涂料失效后一两年也不会有什么大问题。但事实真的如此吗?这就要从钢铁腐蚀的原因说起。

俄巡洋舰带着锈蚀执行任务
钢铁广泛用于工业各行各业,但是不可避免的,在空气中暴露一段时间就会生锈。这是因为铁和氧本身就是一对,在自然界中是以稳定的铁矿石(Fe₂O₃/Fe₃O₄)的形式存在。铁矿石属于陶瓷材料,本身硬度(5~6)大于铁的硬度(4~5),但缺乏韧性、不具备可铸造性,无法直接作为生产生活工具为人类所用。为了运用钢铁的结构特性,人们通过冶金工艺手段,将铁与氧剥离开来,形成高纯度的铁与碳、镍、铬等元素的合金,这就形成了现在我们所熟悉的钢铁。

自然界中稳定存在的铁矿石

现在的钢板
虽然铁和氧结合需求迫切,但是我们的船舶都有好好的刷油漆呀,甚至一些船还用上了不锈钢和铝合金等平时不会出现锈迹的材质,为什么船舶还会发生锈蚀呢?这是因为常用的环氧、聚氨酯、丙烯酸等涂层是树脂和固化剂发生交联反应形成的,这种交联形成的结构,会存在一定的孔隙率,使得水分子通过渗透压作为驱动力,侵入到涂层内部,进而到达钢铁表面发生腐蚀。
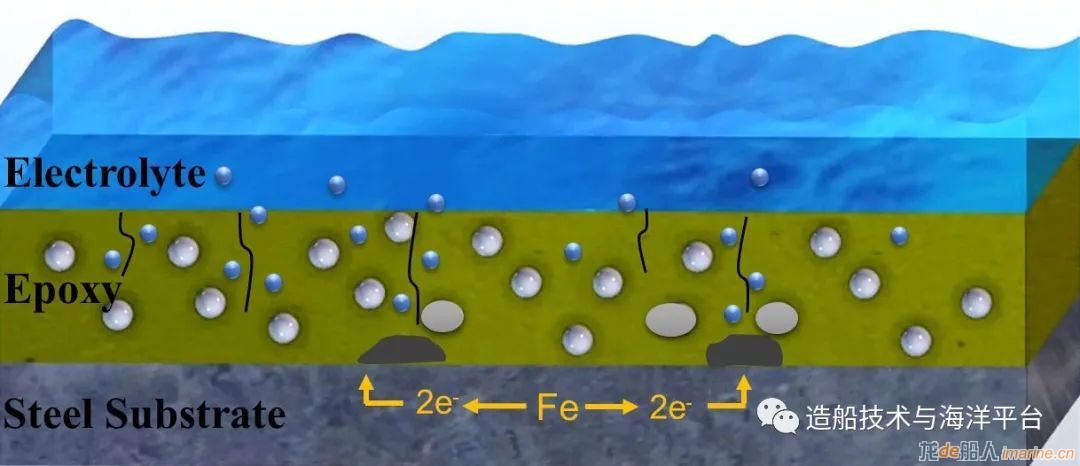
腐蚀介质通过涂层空隙渗透图
高分子结构图
而像不锈钢、铝合金等材质,在日常生活中使用时,一直能够保持明亮的金属光泽,这是因为铝合金表面在空气中很容易形成致密的氧化膜,而不锈钢是由于在钢中加入了大量的铬元素(通常铬的添加量在12wt.%以上,常见的SUS 304不锈钢铬含量为18-20wt.%),在不锈钢表面形成连续且的Cr₂O₃膜,从而实现保护金属基体的效果。但是这招在海洋中是行不通的,海水中存在大量的Cl-离子,凭借自身身材娇小的特点,很容易穿过钝化膜到达基体表面,并与基体发生反应,随后就会导致局部钝化膜失效,出现点蚀。
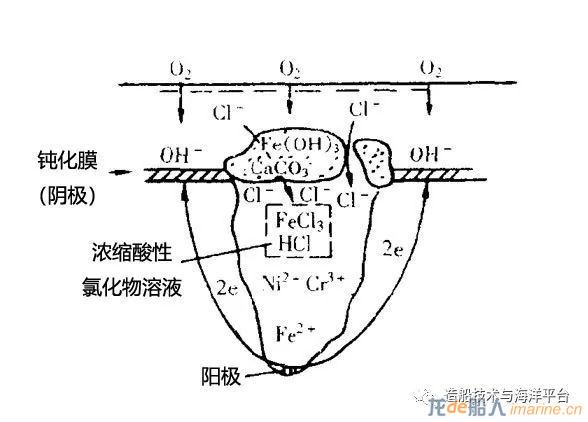
不锈钢点蚀机理示意图
点蚀一旦形成,蚀孔内的金属就处于活化状态,电位较负,作为阳极不断溶解;而点蚀外部的金属表面仍处于钝化状态,电位较正,作为阴极受到保护。这样就在点蚀孔局部形成了腐蚀原电池。蚀孔内主要发生的阳极溶解反应有:
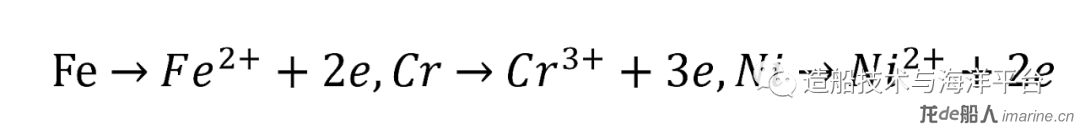
蚀孔外钝化金属表面作为阴极主要发生吸氧反应:
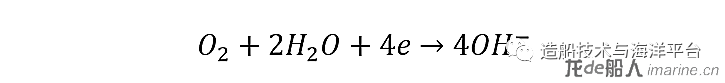
随着阳极不断溶解,腐蚀深度不断加深,阴、阳极彼此分离,二次腐蚀产物在蚀孔口形成Fe(OH)₃,阻碍外部的溶解氧扩散到阳极,在点蚀孔内形成氧浓差电池;同时,内部的金属阳离子也不易扩散出孔外,造成孔内大量的正电荷聚集,并与Cl-形成氯化物和H+。H+浓度的持续增加使得点蚀孔底部呈现出强酸性环境,大幅加速金属腐蚀溶解,使得点蚀孔越来越深,直至腐蚀穿孔。
点蚀由于其特殊的动力学过程,伴随着点蚀发展,蚀孔内形成酸性环境持续促进点蚀的进一步加深,在这种“自催化”的加速作用下,点蚀一旦发生,孔内溶解速度非常大,所以点蚀的危害性很大,经常突然之间导致事故的发生,是破坏性和隐患较大的局部腐蚀形态之一。点蚀是不锈钢、铝合金一类具有钝化膜的基材在海洋中最为典型最为广泛的一种腐蚀形式,而对于刷好油漆的碳钢船板,涂层也会起到钝化膜类似的作用,发生局部腐蚀。所以说,腐蚀不能只凭借钢板减薄来衡量,当我们看到船体锈迹斑斑的时候,钢板内部可能已经“千疮百孔”了。